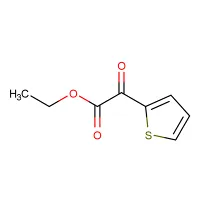
Ethyl 2-oxo-2-(thiofen-2-yl)acetát CAS 4075-58-5
Co je ethyl 2-oxo-2-(thiofen-2-yl)acetát CAS 4075-58-5?
Ethyl 2-oxo-2-(thiofen-2-yl)acetát CAS 4075-58-5 se běžně používá jako reakční substrát nebo činidlo v organické syntéze a lze jej použít k syntéze jiných organických sloučenin, jako jsou thioheterocyklické sloučeniny. Má určitou aktivitu a může se účastnit různých typů chemických reakcí, jako je esterifikace, nukleofilní substituce atd.
Proč si vybrat nás
Naše továrna
Sichuan Biosynce Pharmaceutical Technology Co., Ltd. byla založena v roce 2008. Biosynce se specializuje na vývoj, dodávky a marketing farmaceutických meziproduktů, API a čistých chemických produktů.
Naše produkty
Naše produkty zahrnují Pyrrole Series, Piperazine Series, Pyridine Series, Chinoline Series a Piperidine Series, také poskytujeme CDMO, CRO a přizpůsobené služby syntézy pro domácí i zahraniční zákazníky.
R&D
Náš výzkumný a vývojový tým je složen z vysoce kvalifikovaných a zkušených lékařů a magistrů s prvotřídním domácím i zahraničním zázemím farmaceutického chemického průmyslu, bohatými zkušenostmi v oblasti výzkumu a vývoje a řízení. Knihovnu produktů můžeme průběžně aktualizovat podle potřeb zákazníků a poskytovat více než tisíce produktů skladem v balení od gramů po tuny a každý den přibývají nové skladové produkty.
Produkční trh
Biosynce má nezávislé výzkumné a vývojové a kontrolní středisko, které přísně testuje kvalitu produktů a poskytuje zákazníkům vysoce kvalitní produkty, naše produkty jsou široce vyváženy do Severní Ameriky, Evropy, Asie a Afriky. Naším cílem je navázat dlouhodobé a vzájemně výhodné vztahy se zákazníky a nabízet vynikající produkty a služby.
Vzhledem k jejich vysoké stabilitě vznikají thiofeny z mnoha reakcí zahrnujících zdroje síry a uhlovodíky, zejména nenasycené. První syntéza thiofenu od Meyera, ohlášené ve stejném roce, kdy učinil svůj objev, zahrnuje acetylen a elementární síru. Thiofeny se klasicky připravují reakcí 1,4-diketonů, diesterů nebo dikarboxylátů se sulfidizačními činidly, jako je P4S10, jako v Paal-Knorrově syntéze thiofenu. Specializované thiofeny lze syntetizovat podobně pomocí Lawessonova činidla jako sulfidizačního činidla nebo pomocí Gewaldovy reakce, která zahrnuje kondenzaci dvou esterů v přítomnosti elementární síry. Další metodou je Volhard-Erdmannova cyklizace.
Thiofen se celosvětově vyrábí ve skromném měřítku kolem 2,000 metrických tun ročně. Výroba zahrnuje reakci parní fáze zdroje síry, typicky sirouhlíku, a zdroje C-4, typicky butanolu. Tato činidla jsou uvedena do kontaktu s oxidovým katalyzátorem při 500–550 stupních.
Specifikace ethyl 2-oxo-2-(2-thienyl)acetátu
Ethylthiofen-2-glyoxylát (4075-58-5) může být také nazýván Ethyl-2-thiofeneglyoxylát; ethyl-alfa-oxothiofen-2-acetát; ethylester kyseliny thiofen-2-glyoxylové; Ethyl 2-oxo-2-(2-thienyl)acetát .Je nebezpečný, takže opatření první pomoci a další by měla být známa. Jako například: Na kůži: nejprve opláchněte kůži okamžitě zapijte velkým množstvím vody po dobu nejméně 15 minut a odstraňte kontaminovaný oděv. Za druhé, získejte lékařskou pomoc v obuvi. Nebo v očích: Vyplachujte oči velkým množstvím vody po dobu alespoň 15 minut, občas nadzvedněte horní a spodní víčko. Poté brzy vyhledejte lékařskou pomoc. Při nadýchání: Přemístěte se z místa expozice a přesuňte se na čerstvý vzduch. Zajistěte umělé dýchání. nedýchá. Při obtížném dýchání podejte kyslík. A jakmile seženete lékařskou pomoc. Poté dojde k požití produktu: Vypláchněte ústa vodou a okamžitě vyhledejte lékařskou pomoc. Poznámky pro lékaře: Léčte podpůrně a symptomaticky.
Ethylthiofen-2-glyoxylát (4075-58-5) může být navíc stabilní za normálních teplotních a tlakových podmínek. Není kompatibilní se silnými oxidačními činidly, zdroji vznícení, silnými kyselinami, silnými zásadami a nesmíte berte jej s nekompatibilními materiály. A také zabraňte jeho rozkladu na nebezpečné produkty rozkladu: dráždivé a toxické výpary a plyny, oxid uhličitý, oxid uhelnatý.
Terapeutický význam syntetického thiofenu
Thiofen a jeho substituované deriváty jsou velmi důležitou třídou heterocyklických sloučenin, které vykazují zajímavé aplikace v oblasti lékařské chemie. Pro lékařské chemiky se stala nepostradatelnou kotvou pro vytváření kombinatorické knihovny a provádění vyčerpávajícího úsilí při hledání molekul olova. Uvádí se, že má širokou škálu terapeutických vlastností s různými aplikacemi v lékařské chemii a materiálové vědě, což přitahuje velký zájem v průmyslu i akademické sféře.
Bylo prokázáno, že jsou účinnými léky v současném příslušném scénáři onemocnění. Jsou to pozoruhodně účinné sloučeniny jak s ohledem na jejich biologické a fyziologické funkce, jako jsou protizánětlivé, antipsychotické, antiarytmické, anti-úzkostné, antimykotické, antioxidační, modulující estrogenové receptory, antimitotické, antimikrobiální, kinázy inhibující a protirakovinné.
Syntéza a charakterizace nových thiofenových skupin s širší terapeutickou aktivitou je tedy tématem zájmu pro lékařské chemiky, aby syntetizovali a zkoumali nové strukturální prototypy s účinnější farmakologickou aktivitou. Nicméně několik komerčně dostupných léků, jako je Tipepidin, Tiquizium Bromides, Timepidium Bromide, Dorzolamid, Tioconazole, Citizolam, Sertaconazole Nitrate a Benocyklidin, také obsahuje thiofenové jádro.
Thiofen byl objeven jako kontaminant v benzenu. Má molekulovou hmotnost 84,14 g/mol, hustotu 1,051 g/ml a bod tání - 38 stupňů. Je rozpustný ve většině organických rozpouštědel, jako je alkohol a ether, ale nerozpustný ve vodě. "Elektronové páry" na síře jsou výrazně delokalizovány v systému π elektronů a chová se extrémně reaktivní jako derivát benzenu. Thiofen tvoří azeotrop s ethanolem jako benzen. Podobnost mezi fyzikálně-chemickými vlastnostmi benzenu a thiofenu je pozoruhodná. Například bod varu benzenu je 81,1 stupně a bod varu thiofenu 84,4 stupně (při 760 mmHg), a proto jsou oba dobře známým příkladem bioisosterismu. Může být snadno sulfonován, nitrován, halogenován, acylován, ale nemůže být alkylován a oxidován.
V lékařské chemii jsou deriváty thiofenu velmi důležité heterocykly, které vykazují pozoruhodné aplikace v různých oborech. V lékařství vykazují deriváty thiofenu antimikrobiální, analgetickou a protizánětlivou, antihypertenzní a protinádorovou aktivitu, přičemž se také používají jako inhibitory koroze kovů nebo při výrobě světelných diod v materiálové vědě.
Molekulární a krystalové struktury a spektroskopické vlastnosti kyseliny 2-oxo-2-(thiofen-2-yl)ethylfosfonové
Deriváty kyseliny fosfonové našly uplatnění při skladování energie a katalýze. Byly také použity při iontové výměně, enantioselektivních interkalačních reakcích a při samoskládání tenkých filmů vykazujících elektroaktivní vlastnosti. Kromě toho byly také vyvinuty polyelektrolytové membrány na bázi derivátů kyseliny fosfonové a bylo prokázáno, že vykazují značnou odolnost vůči teplotě a korozi, jakož i vůči útokům volných radikálů.
Deriváty kyseliny fosfonové jsou také zajímavými sloučeninami ze zásadnějšího hlediska. Ve skutečnosti vnitřní konformační flexibilita jejich hydroxylových skupin a také jejich schopnost účastnit se intra- a/nebo intermolekulárních interakcí typu H-vazeb, jak jako akceptory, tak jako donory, obvykle vedou k zajímavým molekulárním a supramolekulárním architekturám. Ty jsou posíleny v případech, kdy substituent připojený ke skupině fosfonové kyseliny má také strukturní charakteristiky náročné na výzkum (např. konformační flexibilita, delokalizace π-elektronu, schopnost vytvářet H-vazbu, mimo jiné).
Je popsána syntéza nové kyseliny fosfonové, kyseliny (2-oxo-2-(thiofen-2-yl)ethyl)fosfonové (OTEPA; schéma 1), spolu s její strukturní a spektroskopickou charakterizací na molekulární úrovni a v krystalické fázi. OTEPA je jednoduchý derivát kyseliny fosfonové, který odpovídá strukturním charakteristikám pro zobrazení značného počtu konformerů (má pět různých stupňů vnitřní rotace, které mohou vést ke konformačním izomerům) a různé typy interakcí typu H-typu uvnitř/vnitromolekulárně [zobrazuje pět elektronegativní centra, plus delokalizovaný kruhový π-systém, který může fungovat jako akceptory H-vazby (donory elektronů) a dvě OH skupiny, které mohou fungovat jako donory H-vazby].
Hlavním cílem tohoto článku je osvětlit různou důležitost hlavních intra- a intermolekulárních interakcí existujících v izolované molekule sloučeniny a/nebo v krystalické fázi. Tyto údaje jsou důležité pro zlepšení dostupných znalostí o strukturních charakteristikách a vlastnostech skupiny fosfonové kyseliny. teoreticky byl zkoumán konformační prostor molekuly OTEPA a strukturně a spektroskopicky byly charakterizovány nejstabilnější konformery. Relativní stability konformerů jsou vysvětleny na základě strukturních znaků sloučeniny, přičemž intramolekulární H-vazba vytvořená mezi jednou z OH skupin fragmentu fosfonové kyseliny a karbonylovým atomem kyslíku substituentu je hlavní intramolekulární interakcí odpovědnou za stabilizace konformerů s nejnižší energií sloučeniny.
Velmi zajímavé je, že kontakt O⋯S mezi karbonylovým atomem kyslíku a atomem síry thiofenového kruhu (který je podobný kontaktu typu N⋯S nalezenému dříve v jiných molekulárních systémech) byl také zjištěn jako důležitá intramolekulární interakce při určování stabilita dvou konformerů OTEPA s nejnižší energií. Na druhé straně v krystalu je intramolekulární H-vazba stabilizující konformery s nejnižší energií izolované molekuly OTEPA nahrazena intermolekulárními H-vazbami vytvořenými se sousedními molekulami, takže vybrané konformace v krystalické fázi jsou struktury s vyšší energií. zatímco izolovaný (s energiemi vyššími než nejstabilnější konformer o více než 13 kJ mol−1). OTEPA je pak zajímavým příkladem sloučeniny vykazující konformační selekci po krystalizaci, která vyžaduje značnou strukturní reorganizaci.
Biosynce má nezávislé výzkumné a vývojové a kontrolní středisko, které přísně testuje kvalitu produktů a poskytuje zákazníkům vysoce kvalitní produkty, naše produkty jsou široce vyváženy do Severní Ameriky, Evropy, Asie a Afriky. Naším cílem je navázat dlouhodobé a vzájemně výhodné vztahy se zákazníky a nabízet vynikající produkty a služby.

FAQ
Populární Tagy: ethyl 2-oxo-2-(thiofen-2-yl)acetát cas 4075-58-5, čínský ethyl 2-oxo-2-(thiofen-2-yl) )acetát cas 4075-58-5 výrobci, dodavatelé, továrna
Dvojice
NeMohlo by se Vám také líbit
Odeslat dotaz